이번 포스팅은 가역단열과정에 대해 알아보겠습니다.
단열이라는 조건은 어떠한 계에서 외부와의 열 교환을 단절한다의 단열입니다.

위 두 그래프를 통해 보면 단열이 어떤 의미인지 알 수 있습니다.
1. 엔트로피
우선 엔트로피를 나타내는 클라우시우스 부등식에 대해 간단히 알아야 합니다.
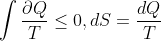

위 1번식이 클라우시우스 부등식인데,
이 식의 의미는 계에 전달되는 열량은 미소의 열전달의 합으로 볼 수 있으므로
적분은 미소 열전달을 경계면의 절대온도로 나눈 값들의 합이라고 볼 수 있습니다.
엔트로피는 추후에 디테일하게 다루어 보겠습니다.
2. 가역단열과정 유도
이제 가역단열과정에 대해 알아보겠습니다.
우선 이전에 포스트 한 내부에너지를 가지고 옵니다,

이 식은

이렇게 표현할 수 있습니다.
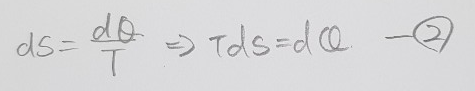
그리고 앞서 언급한 엔트로피 식을 정리해 줍니다.

그리고 W일 을 위 식으로 표현해 주고
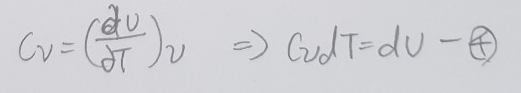
마지막으로 정적비열 식을 정리해 준다음에 2번 3번 4번식을 1번식에 대입하게 되면
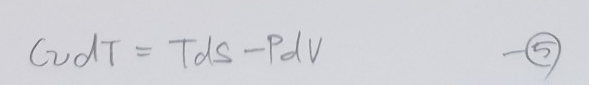
위와 같이 정리가 됩니다. 그리고 각 항을 T로 나누어 주면

이 됩니다.

또한 여기서 단열 조건이기에, 즉 Q인 열출입이 없으므로, S역시 0이 됩니다.
이상기체 방정식을 압력에 관한 식으로 정리해주면 (n은 몰수이기에 대부분 1로 간주합니다)
위 식이 도출 됩니다. 또한 이 식을 정리해주면
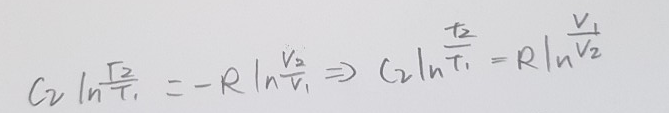
가 되는데, 앞서 정적비열과 정압비열 포스트에서 서로의 관계를 확인해보았습니다. 그러므로
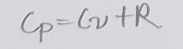
를 대입하면 최종적으로

이 도출되게 됩니다.
여기서 PV=RT의 이상기체 방정식을 V에 관해 정리해서 풀이하게 되면

이 도출됩니다.
'전공 > 열역학' 카테고리의 다른 글
| 열역학 #10 카르노 기관 (1) | 2020.08.24 |
|---|---|
| 열역학 #9 가역과정, 비가역과정 (0) | 2020.08.24 |
| 기계공학 취준일기 전공편 #7 정적비열과 정압비열 (0) | 2020.08.23 |
| 기계공학 취준일기 전공편 #6 내부에너지, 엔탈피, 축일 (0) | 2020.08.23 |
| 기계공학 취업일기 전공편 #1 열역학적 계 (2) | 2020.08.13 |